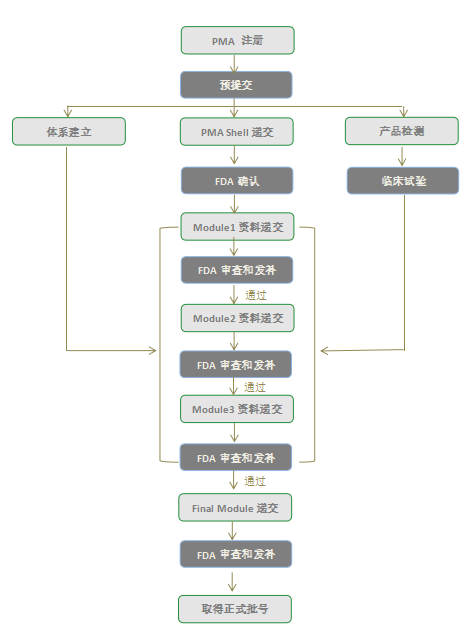
PMA申请可以分为新的PMA申请和PMA补充申请,其中新的PMA申请是指申请人对所生产的从未被FDA批准过的新产品提出的申请,而PMA补充申请则是申请人拟对一个已批准PMA申请的产品进行影响安全性和有效性的改变前提出的申请。在美国,针对高风险的III类医疗器械,或者无法和现有的I类,II类和III类(需要510(k)申请的III类产品)建立实质等同的器械,都需要在上市前向美国食品药品监督管理局(FDA)递交上市前批准(Premarket Approval, PMA)的申请,并获得FDA的批
PMA是FDA针对医疗器械三个控制等级中最严格的一种,FDA会对上市前的工厂检查结果,产品技术,非临床测试结果及临床实验进行科学和法规的审核,并召集专家委员会咨询意见,以判定是否有充分、有效、科学的证据确保产品在其预期用途范围内的安全性和有效性。